Agence de presse Xinhua, Tianjin (Reporters Zhang Jianxin, Li Yating) L'équipe de Liu Shulin, chercheur à l'École de chimie de l'Université de Nankai en Chine, a récemment développé avec succès une nouvelle voie anti-virus de la grippe à large spectre. Cette stratégie perturbe fondamentalement l’avantage évolutif du virus en dégradant de manière synchrone plusieurs composants clés au cœur de la réplication virale, jetant ainsi une base solide pour le développement de la prochaine génération de médicaments antigrippaux puissants, durables et à large spectre. Des résultats de recherche pertinents ont été récemment publiés dans la revue universitaire internationale « Journal of the American Chemical Society ».
Selon l'équipe de recherche, les virus de la grippe A peuvent facilement échapper aux réponses immunitaires de l'hôte et aux médicaments existants en raison de leur taux de mutation élevé. Les médicaments antiviraux actuellement utilisés en clinique ne peuvent généralement cibler qu’une seule cible du virus, ce qui permet au virus de développer facilement une résistance aux médicaments par mutation, ce qui entraîne un effet médicamenteux considérablement réduit et une efficacité à large spectre limitée. De nouvelles stratégies de traitement sont nécessaires de toute urgence dans le monde entier.
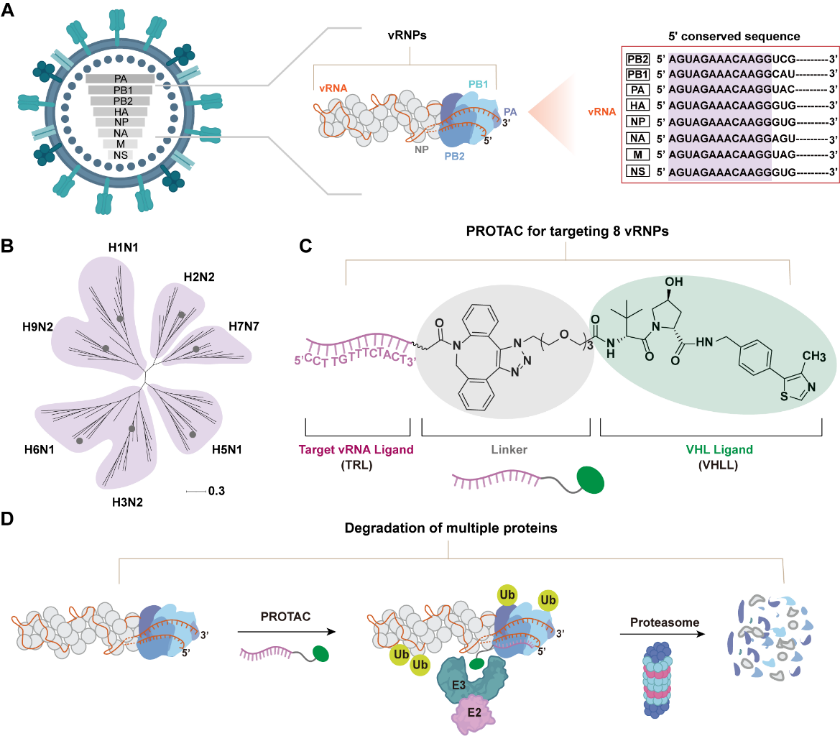
Diagramme schématique de la dégradation médiée par PROTAC des protéines multivirales. L'agence de presse Xinhua a rapporté que Liu Shulin a expliqué que l'équipe avait développé une stratégie antivirus appelée « Multiplex PROTAC ». Son mécanisme central réside dans l'utilisation intelligente d'une région 5' non traduite hautement conservée dans l'ARN viral de ciblage, considérée comme le « code universel ». Sur cette base, les chercheurs de leur équipe ont conçu une molécule PROTAC multifonctionnelle. Une extrémité de la molécule peut reconnaître et lier avec précision le « code universel » du virus, et l’autre extrémité est responsable du recrutement du protéasome, le système de dégradation des protéines inhérent aux cellules humaines. Cette conception fait que la molécule agit comme un « cheval de Troie ». Après avoir pénétré dans une cellule infectée, il peut s'accrocher au complexe ribonucléoprotéique viral, au noyau de la réplication virale, et au « broyeur » de la cellule en même temps, marquant ainsi la protéine centrale du virus comme une marque de « destruction », puis guidant la machinerie cellulaire pour dégrader complètement ces éléments clés de la réplication virale, détruisant ainsi la capacité de réplication du virus à partir de la source.
Les résultats expérimentaux de l’équipe montrent que la stratégie multiple PROTAC présente d’excellentes performances antivirales. Non seulement il peut inhiber efficacement la réplication virale de manière dépendante de la concentration, mais son effet inhibiteur peut durer plus de 48 heures. Sa persistance et son efficacité sont nettement meilleures que celles des médicaments témoins à cible unique. Ce qui est particulièrement critique est que cette stratégie réussisse à construire une barrière de résistance génétique élevée en dégradant de manière synchrone plusieurs protéines virales. Cela signifie que si le virus veut s’échapper, il doit avoir des mutations d’évasion efficaces sur plusieurs cibles clés en même temps. Cela constitue un obstacle insurmontable pour le virus dans son évolution naturelle et réduit le risque de résistance aux médicaments. En outre, cette stratégie a montré une activité à large spectre contre plusieurs souches de grippe, soulignant son potentiel en tant que médicament anti-grippe à large spectre.
Les évaluateurs ont fait remarquer que la polyvalence de cette stratégie offre également une nouvelle voie technique et un nouvel espace d'imagination pour faire face à d'autres virus à mutation rapide à l'avenir.